アルツハイマー病治療薬 レカネマブ(レケンビ®)、ドナネマブ(ケサンラ®)治療についてお知らせ
アルツハイマー病治療薬レカネマブ(レケンビ®)が2023年12月20日に、ドナネマブ(ケサンラ®)が2024年11月26日に発売となりました。
どちらも、アミロイドβと呼ばれるタンパク質を脳内から除去する新しい作用をもった薬剤です。当院脳神経外科では、厚生労働省が定めた「最適使用推進ガイドライン」に従い、安全に投与できる体制を整えています。受診からの流れをご参照いただき、治療をご希望の際には脳神経外科外来までご連絡ください。
愛宕病院で行っている抗アミロイドβ抗体薬に関する診療のご案内パンフレットは、こちらからご覧いただけます。
レケンビ®・ケサンラ®に関する診療のご案内(2026年2月作成)※PDFファイルが開きます
認知症高齢者の数はますます増加
65歳以上の高齢者のうち認知症を発症している人は推計15%で、2012年時点で約462万人に上ることが厚生労働省研究班の調査で明らかになっています。認知症の前段階である軽度認知障害(MCI)の高齢者も約400万人いると推計されており、65歳以上の4人に1人が認知症とその“予備軍”となる計算です。

※出所:「日本における認知症の高齢者人口の将来推計に関する研究」
(平成26年度厚生労働科学研究補助金特別研究事業 九州大学 二宮教授)による速報値
厚生労働省 認知症施策の現状について
※2015年以降のMCIの推計値は2012年の推計値をもとに認知症の人数86%として計算
さらに、2015年1月厚生労働省により、2025年の認知症患者は700万人を超えるとの推計が発表されました。これにMCI患者数を加えると、約1300万人となり、65歳以上の3人に1人が認知症患者とその予備軍といえることになりそうです。
また、認知症専門医の間では、MCIの数はもっと多いはずだという声も多く、MCI患者だけで1500万人を超えるという見解を持っている医師も少なくはないようです。
主な認知症の種類別割合
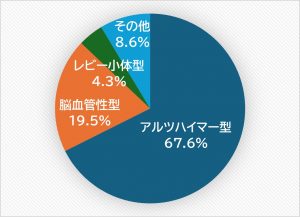
※出典:厚生労働科学研究費補助金認知症対策総合研究事業「都市部における認知症有病率と認知症の生活機能障害への対応」平成23年度~24年度 総合研究報告書
認知症の種類によって症状も変わってくるので、それぞれに合わせた適切な対応やケアが重要になります。
軽度認知障害(MCI)とは?
MCI(Mild COgnitive Impairment)とは、認知症と完全に診断される一歩手前の状態のことです。放っておくと認知症に進行しますが、適切な予防をすることで健常な状態に戻る可能性があります。
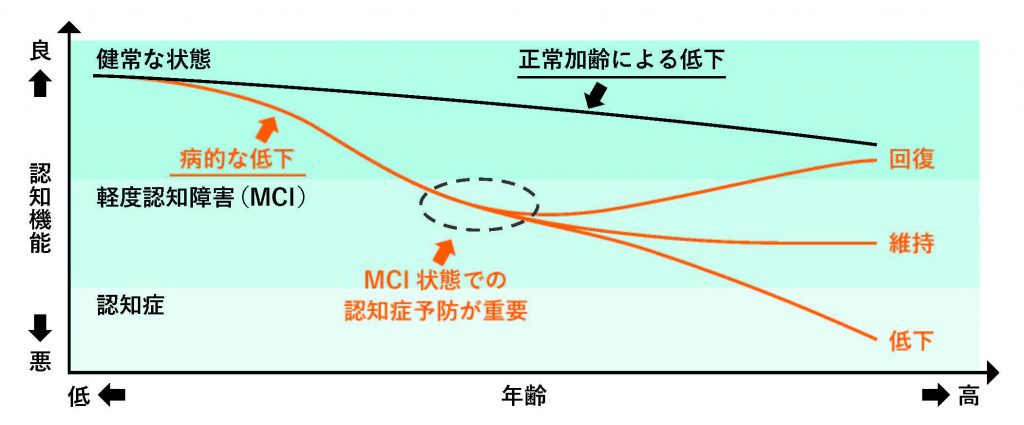
※出典:厚生労働省「MCIハンドブック」
軽度認知障害(MCI)の主な原因
MCIから認知症に進みやすい原因の一つにアルツハイマー病がありますが、脳の病気だけでなく、体の病気や精神的なストレスなどさまざまな原因があげられます。
原因を早期に発見して、MCIから認知症へ進行しないよう適切な対策を行うことが重要です。
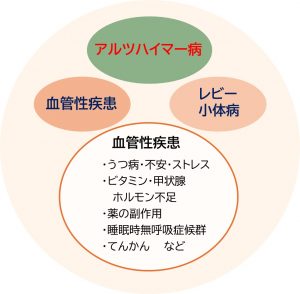
日本神経学会監修:認知症疾患診療ガイドライン2017(医学書院)p6,2017
Alzheimer’s Society. Factsheet 470LP June2019
https://www.alzheimers.org.uk/sites/default/files/2019-09/
470lp-what-is-mild-cognitive-impairment-mci-190521.pdfより作成
アルツハイマー病とは
病理学的にアミロイド(Aβ amyloidosis;大脳皮質、脳血管)と神経原線維変化(neurofibrillary tangle)の2つの変化を特徴とし、神経細胞の障害、細胞死を生じます。
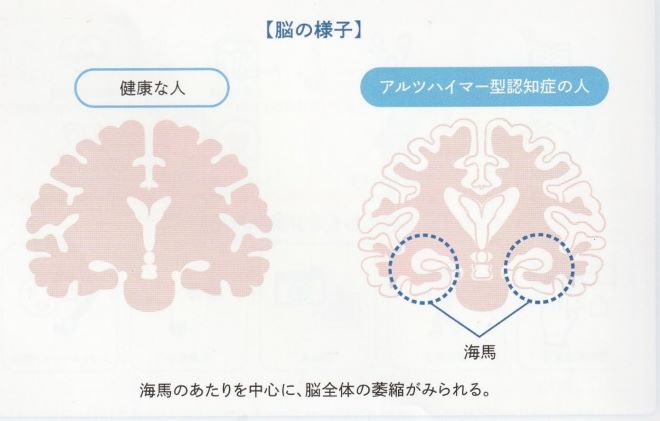
脳の萎縮が記憶の中枢である海馬およびその周辺から始まり、拡がっていくため、症状は記憶の障害(もの忘れ)から始まります。
主要症状は緩徐進行性の出来事記憶(episodic memory)障害に始まる記憶と学習の障害が典型的で、失語、遂行機能障害、視空間認知障害、人格変化などの社会的認知機能の障害に進展します。
アルツハイマー病の進行

出典:エーザイ株式会社「レケンビ®の治療を始める方とそのご家族へ」
アルツハイマー病による軽度認知障害(MCI)
アルツハイマー病によるMCIと認知症のちがい

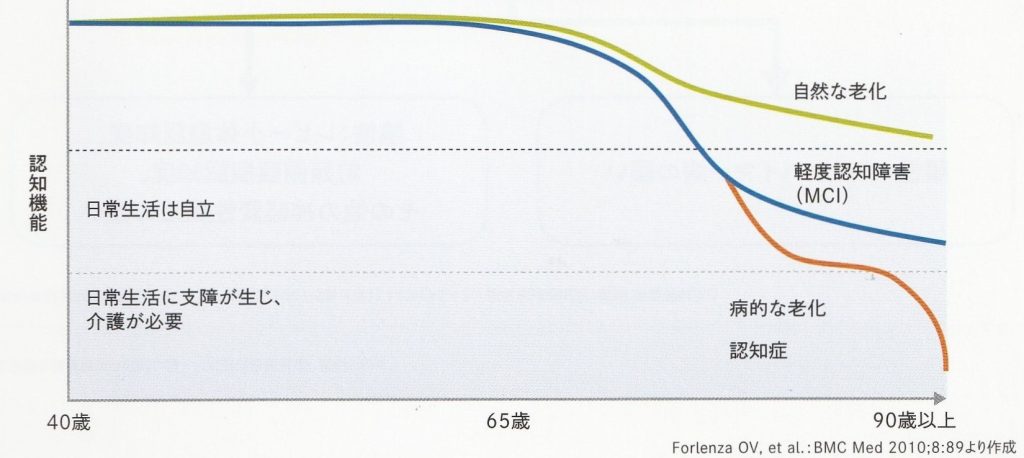
年齢に応じた認知機能の変化
認知症新時代
「レケンビ®」(一般名:レカネマブ)は、「アルツハイマー病による軽度認知障害及び軽度の認知症の進行抑制」の効能・効果で製造販売承認を取得して2023年12月20日にエーザイ株式会社から発売。日本での販売は米国に次いで2か国目になります。
また、米国のイーライリリー社から、早期アルツハイマー病の治療薬として、抗アミロイド医薬「ケサンラ®」(一般名:ドナネマブ)が2024年11月26日に発売されました。
抗アミロイドβ抗体薬
- 「レケンビ®」「ケサンラ®」は、アミロイドβモノクローナル抗体であり、アルツハイマー病の進行を抑制し、認知機能と日常生活機能の低下を遅らせることを実証し承認された世界で初めての治療薬です。
- 「今までの認知症の薬物治療とはまったく違う、大きなブレイクスルー(突破口)になる。(アルツハイマー病を含む)神経変性症の治療を変える大きな一歩だ」
日本老年精神医学会理事長 大阪大学 池田学教授(精神医学)
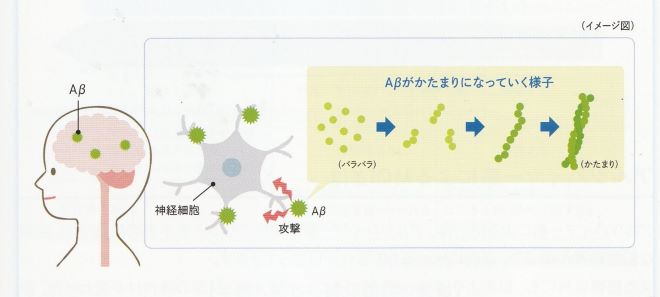
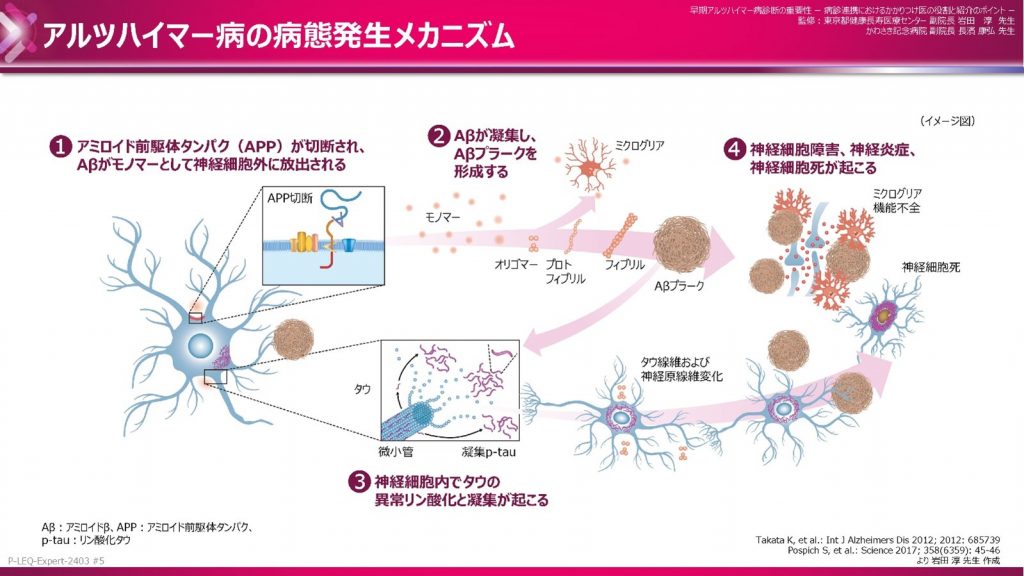
アルツハイマー病は、脳におけるアミロイドβと呼ばれるタンパク質の異常が病気を引き起こします。
正常な状態では、アミロイドβは産生されてもバラバラのまま脳から取り除かれますが、アルツハイマー病の場合は塊を作って脳の中にたまります。この塊が神経細胞を障害することで、神経細胞の働きが落ち、数が減って脳の萎縮が進みます。
抗アミロイドβ抗体薬は、アミロイドβに結合し、これを減少させることで病気の進行を抑制します。
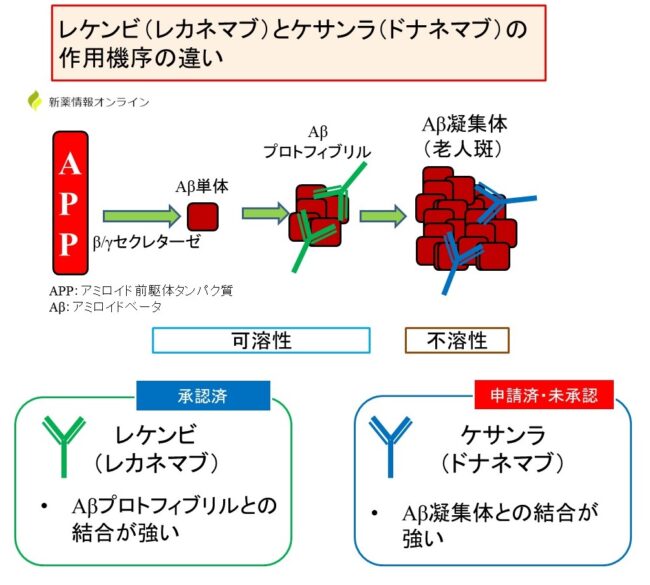
出典:新薬情報オンライン URL:https://passmed.co.jp/di/archives/16970
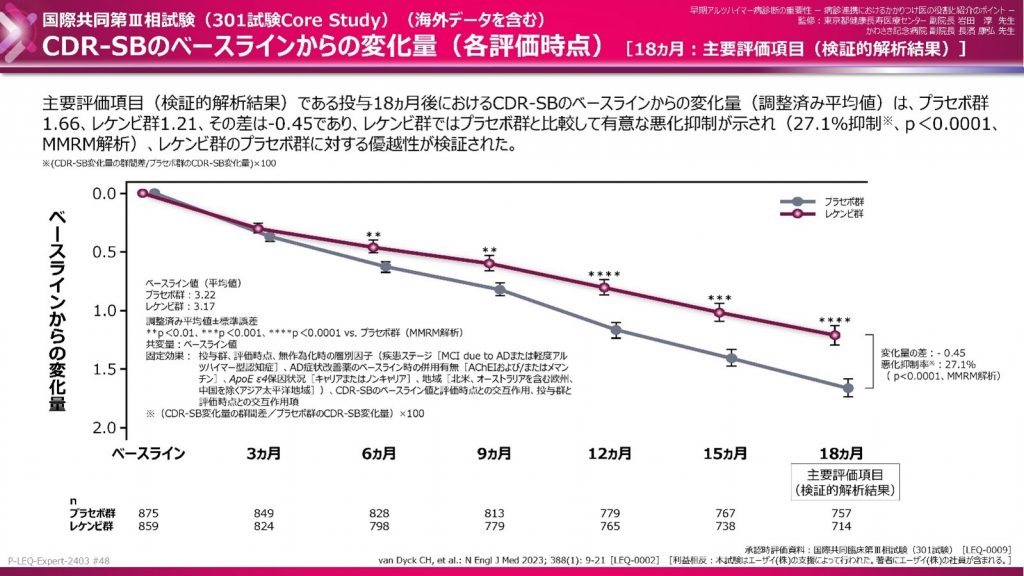
発症早期の患者、約1800人を対象に実施した最終段階の臨床試験(治験)結果によると、レケンビ®を投与した患者は、偽薬を投与した患者に比べ、1年半後の症状進行を27%抑制。試算では中等度の患者の症状進行を平均2~3年遅らせる可能性があると報告されています。
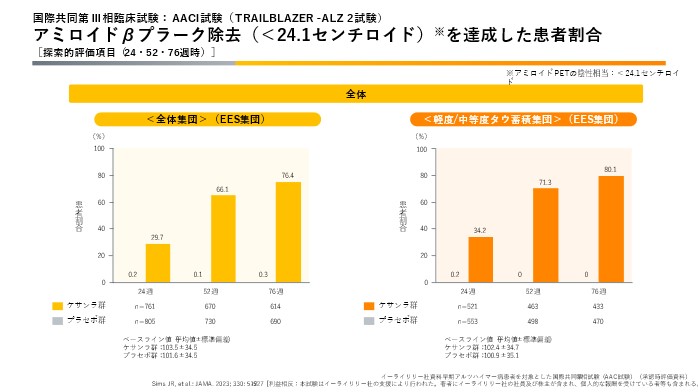
ケサンラ®を投与した患者は、投与12ヶ月で66.1%の方が、投与18ヶ月で76.4%の方がアミロイドβプラークが陰性となりました。

出典:新薬情報オンライン URL:https://passmed.co.jp/di/archives/16970
抗アミロイドβ抗体薬は厚生労働省が定めた「最適使用推進ガイドライン」を守って使用することとなっています
投与対象となる患者
①治療意思の確認
②本剤の禁忌に該当しない
③MRI検査(1.5テスラ以上)が実施可能
④認知機能の低下および臨床症状の重症度範囲
a)認知機能評価 MMSEスコア 22~30点(レケンビ®)・20~28点(ケサンラ®)
b)臨床認知症尺度 CDRスコア 全般スコア0.5または1
⑤アミロイドPETまたは脳脊髄液(CSF)検査を実施し、アミロイドβ病理を示唆する所見が確認されている
投与施設
ア 初回投与に際して必要な体制
(ⅰ)施設における医師の配置
(ⅱ)検査体制
(ⅲ)チーム体制
イ 院内の医薬品情報管理の体制
ウ 副作用への対応
受診から検査と治療の流れ
STEP1 MCI・認知症であるか否かを診断します
受診時には、家族、介護者など患者の日常の様子を知る人の同行が必要です。
認知機能検査(MMSE・CDR)を受けていただきます。
STEP2 MCI・認知症の原因を調べます
血液検査・脳MRI撮影を行い、検査結果を総合して鑑別診断します。
MRIでは抗アミロイドβ薬の副作用リスクの高い特有の異常がないことを確認します。
STEP3 アルツハイマー病の診断・抗アミロイドβ薬の適応か否かの検査をします
脳へのアミロイドβの蓄積を証明する検査として、腰椎穿刺による髄液検査を行います。
陽性であれば抗アミロイドβ薬の投与の対象に該当するか否かを判断します。
投与スケジュール
2週間に一度来院していただき、静脈点滴で薬剤を投与します。点滴にかかる時間は約1時間です。
投与開始から半年程度は、脳の腫れや脳の出血などの副反応を生じる可能性があるため、定期的な脳MRI検査を行います。
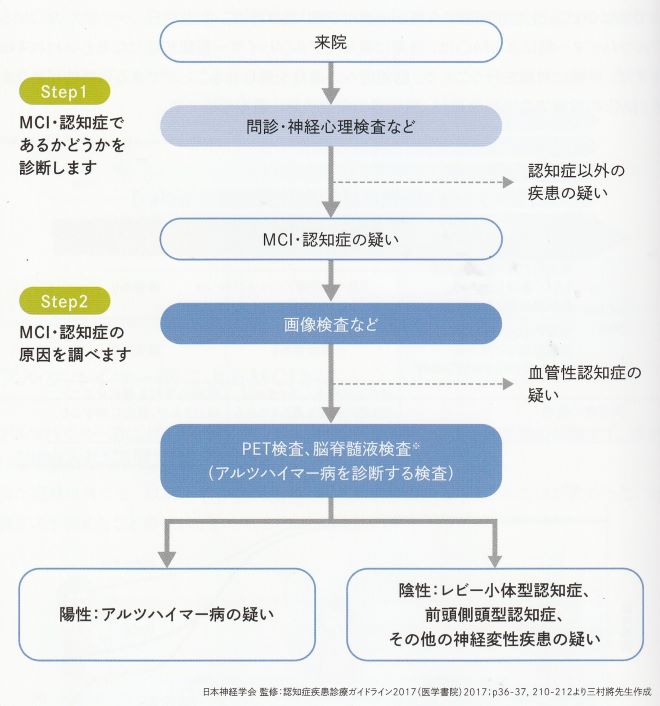
PET検査(アミロイドPET)と脳髄液検査
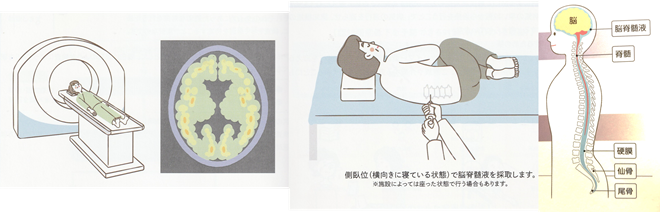
PET検査は被爆の影響があり、抗アミロイドβ薬の要否を判断する目的で行う場合に保険適用となりました。
髄液検査は局所麻酔で行い、10分程度で終わります。脳神経外科では日常的に行っている検査です。
抗アミロイドβ薬の副作用
- 抗アミロイドβ薬のようにアミロイドβを減少させる薬を使用すると、アミロイド関連画像異常(ARIA)という副作用があらわれることがあります。
- ARIAは、脳からアミロイドβが除去されるときに、一時的に血液や血漿が血管の外に漏れだすことで起こります。それにより、脳のむくみや脳の中で出血が起こることがあります。(症候性はまれ)
-
- ARIAの有無はMRI検査で確認することができるので、抗アミロイドβ薬投与後は、MRI検査を定期的に行います。
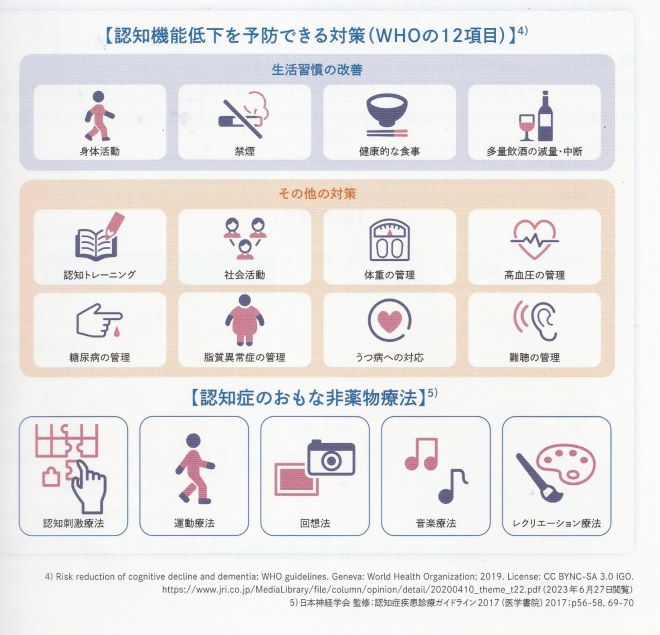
アルツハイマー病の非薬物療法(薬を使わない治療)
-
-
- 体の健康:睡眠、食事や運動などの生活習慣。生活習慣病の治療。
- 心の健康:明るい気持ちでいる。心配や不安は相談。
- 交流・コミュニケーション:社会参加、仕事や習い事を続ける。ボランティア活動、周囲の人と交流する。
- 生活上の工夫:おおらかに考える。メモや手帳でもの忘れに備える。
-
非薬物療法(薬を使わない治療)